Роль витамина D3 в развитии фолликулов
Аннотация
Время прочтения 40 мин
Витамин D3 играет важную роль в женской репродуктивной системе. По мере накопления данных механизмы его влияния на развитие фолликулов активно изучаются. В яичниках были обнаружены ключевые ферменты, участвующие в синтезе и метаболизме витамина D3, что указывает на возможность его локального синтеза и метаболизма в ткани яичника. Кроме того, выявление рецепторов витамина D (VDR) в фолликулах свидетельствует о том, что витамин D3 может реализовывать свои эффекты через специфическое связывание с этими рецепторами в процессе фолликулогенеза.
Дальнейшие исследования показали, что витамин D3 способствует росту фолликулов за счёт стимуляции развития гранулёзных клеток (GCs) и ооцитов. В настоящее время механизмы действия витамина D3 при развитии фолликулов становятся всё более понятными. Витамин D3 поддерживает развитие ооцитов, регулируя молекулы, участвующие в поддержании мейотического ареста. Он также усиливает пролиферацию гранулёзных клеток посредством стимуляции синтеза стероидных гормонов и регуляции клеточного цикла.
Кроме того, витамин D3 оказывает противовоспалительное действие, снижая выраженность оксидативного стресса и уровень конечных продуктов гликирования (AGEs), что способствует уменьшению негативного влияния воспаления на развитие фолликулов. Эти свойства витамина D3 находят клиническое применение, в частности при синдроме поликистозных яичников (СПКЯ), для улучшения женской фертильности и повышения эффективности программ экстракорпорального оплодотворения (ЭКО).
В данном обзоре представлены современные данные о роли и механизмах действия витамина D3 в развитии фолликулов, а также кратко рассмотрены его клинические применения.
Дальнейшие исследования показали, что витамин D3 способствует росту фолликулов за счёт стимуляции развития гранулёзных клеток (GCs) и ооцитов. В настоящее время механизмы действия витамина D3 при развитии фолликулов становятся всё более понятными. Витамин D3 поддерживает развитие ооцитов, регулируя молекулы, участвующие в поддержании мейотического ареста. Он также усиливает пролиферацию гранулёзных клеток посредством стимуляции синтеза стероидных гормонов и регуляции клеточного цикла.
Кроме того, витамин D3 оказывает противовоспалительное действие, снижая выраженность оксидативного стресса и уровень конечных продуктов гликирования (AGEs), что способствует уменьшению негативного влияния воспаления на развитие фолликулов. Эти свойства витамина D3 находят клиническое применение, в частности при синдроме поликистозных яичников (СПКЯ), для улучшения женской фертильности и повышения эффективности программ экстракорпорального оплодотворения (ЭКО).
В данном обзоре представлены современные данные о роли и механизмах действия витамина D3 в развитии фолликулов, а также кратко рассмотрены его клинические применения.

08.05.2026

Автор статьи: Дарья Оливко
Специализация: нутрициолог/консультант по питанию.
Член Национального общества диетологов России.
Стаж работы: более 10 лет
Специализация: нутрициолог/консультант по питанию.
Член Национального общества диетологов России.
Стаж работы: более 10 лет
URL скопирован в буфер обмена!
Введение
В организме человека витамин D3 является основной формой витамина D. Он преимущественно синтезируется в коже из 7-дегидрохолестерина под воздействием ультрафиолетового излучения и реализует свои биологические эффекты через связывание с рецепторами витамина D (VDR). Классические функции витамина D3 включают регуляцию кальций-фосфорного обмена, а также поддержку роста и поддержания костной ткани. Кроме того, витамин D3 участвует в регуляции клеточной дифференцировки, воспалительных процессов и апоптоза .
В последние годы всё больше внимания уделяется важной роли поддержания физиологического уровня витамина D3 для нормальной функции яичников и женской репродуктивной системы. Дефицит витамина D связывают с неблагоприятными материнско-фетальными исходами и рядом гинекологических состояний, влияющих на фертильность, включая бесплодие, синдром поликистозных яичников (СПКЯ) и эндометриоз. Кроме того, показано, что добавление витамина D3 у пациенток с СПКЯ способствует снижению инсулинорезистентности, уменьшению уровня андрогенов и повышению частоты наступления беременности. Также витамин D3 может повышать эффективность программ экстракорпорального оплодотворения (ЭКО) у пациенток с бесплодием.
Фолликулы являются основной функциональной единицей яичника и состоят из фолликулярных клеток и развивающегося ооцита. В зависимости от стадии развития выделяют примордиальные, первичные, вторичные, антральные и зрелые фолликулы. По мере развития фолликула прегранулёзные клетки примордиального фолликула постепенно созревают, начиная экспрессировать рецепторы к фолликулостимулирующему гормону, эстрогенам и андрогенам, что соответствует переходу фолликула к гормонозависимой стадии развития. Формирование примордиальных фолликулов и их дальнейшее развитие — ключевые процессы биологии яичников, напрямую определяющие количество доступных ооцитов. Понимание механизмов действия витамина D в процессе фолликулогенеза имеет важное значение для его клинического применения. В следующих разделах рассматриваются современные данные о роли витамина D в регуляции развития и созревания фолликулов, а также возможные сигнальные пути его действия.
В последние годы всё больше внимания уделяется важной роли поддержания физиологического уровня витамина D3 для нормальной функции яичников и женской репродуктивной системы. Дефицит витамина D связывают с неблагоприятными материнско-фетальными исходами и рядом гинекологических состояний, влияющих на фертильность, включая бесплодие, синдром поликистозных яичников (СПКЯ) и эндометриоз. Кроме того, показано, что добавление витамина D3 у пациенток с СПКЯ способствует снижению инсулинорезистентности, уменьшению уровня андрогенов и повышению частоты наступления беременности. Также витамин D3 может повышать эффективность программ экстракорпорального оплодотворения (ЭКО) у пациенток с бесплодием.
Фолликулы являются основной функциональной единицей яичника и состоят из фолликулярных клеток и развивающегося ооцита. В зависимости от стадии развития выделяют примордиальные, первичные, вторичные, антральные и зрелые фолликулы. По мере развития фолликула прегранулёзные клетки примордиального фолликула постепенно созревают, начиная экспрессировать рецепторы к фолликулостимулирующему гормону, эстрогенам и андрогенам, что соответствует переходу фолликула к гормонозависимой стадии развития. Формирование примордиальных фолликулов и их дальнейшее развитие — ключевые процессы биологии яичников, напрямую определяющие количество доступных ооцитов. Понимание механизмов действия витамина D в процессе фолликулогенеза имеет важное значение для его клинического применения. В следующих разделах рассматриваются современные данные о роли витамина D в регуляции развития и созревания фолликулов, а также возможные сигнальные пути его действия.
Метаболизм витамина D3 и экспрессия VDR в яичнике
Обычно витамин D3 превращается в свою биологически активную форму — 1α,25-дигидроксивитамин D3 (1α,25(OH)2D3, кальцитриол) — преимущественно при участии печёночной 25-гидроксилазы и почечной 1-α-гидроксилазы, после чего метаболизируется 24-гидроксилазой. Исследования показали, что помимо классических органов синтеза витамин D3 может локально синтезироваться и в яичнике. 25-гидроксилаза и 1-α-гидроксилаза — ключевые ферменты синтеза кальцитриола, кодируемые генами CYP2R1 и CYP27B1 соответственно. Экспрессия их мРНК обнаружена в яичниках человека и развивающихся фолликулах нечеловекообразных приматов (макак-резусов).
В исследовании фолликулов макак-резусов, культивируемых in vitro, Xu et al. показали, что уровень мРНК CYP2R1 был выше в малых антральных фолликулах по сравнению с преантральными (P < 0,05), тогда как уровень мРНК CYP27B1 существенно не изменялся. В то же время Grzesiak в исследовании фолликулов свиней обнаружил более высокие уровни мРНК и белка CYP27B1 в средних антральных фолликулах по сравнению с малыми антральными фолликулами (мРНК: увеличение в 1,55 раза, P = 0,042; белок: в 2,49 раза, P = 0,005). Кроме того, уровень мРНК CYP24A1 также был выше в средних антральных фолликулах (в 1,96 раза; P = 0,042), тогда как различий по уровню белка между стадиями развития фолликулов не выявлено.
Эти различия могут быть связаны с межвидовыми особенностями и различиями стадий развития анализируемых фолликулов. В совокупности данные указывают на усиление экспрессии ферментов синтеза витамина D3 по мере созревания фолликулов. Кроме того, добавление витамина D3 в культуральную среду приводило к значительному повышению уровня мРНК CYP2R1 в преантральных фолликулах через две недели, что позволяет предположить наличие положительной обратной связи, усиливающей синтез витамина D3 в преантральных фолликулах.
Однако реализация эффектов витамина D3 также зависит от распределения его рецептора — рецептора витамина D (VDR). В присутствии лиганда VDR образует гетеродимерный комплекс с рецептором ретиноидов X (RXR), формируя комплекс VDR/RXR. Этот комплекс связывается с элементами ответа на витамин D в промоторных участках генов-мишеней и регулирует экспрессию генов через каскады сигнальных путей, обеспечивая биологические эффекты.
В 1983 году Dokoh et al. впервые обнаружили экспрессию VDR в яичниках млекопитающих и птиц. Позднее иммуннофлуоресцентное окрашивание VDR было выявлено в ооцитах примордиальных фолликулов у рыб, коз и макак-резусов. В отличие от этого, в первичных и вторичных фолликулах крыс и коз экспрессия VDR преимущественно наблюдалась в гранулёзных клетках (GCs) и тека-клетках (TCs).
В исследованиях ткани яичников макак-резусов Xu et al. использовали иммуногистохимическое окрашивание для оценки экспрессии белка VDR. Было показано, что VDR экспрессируется на всех стадиях развития ооцита. Хотя экспрессия VDR также выявлялась в прегранулёзных клетках примордиальных фолликулов, она была менее выраженной. В гранулёзных клетках первичных фолликулов отмечалось лишь минимальное окрашивание VDR. Однако по мере перехода фолликулов к стадиям вторичных, малых антральных и крупных антральных фолликулов интенсивность окрашивания гранулёзных клеток постепенно увеличивалась. Это указывает на стадийно-зависимый характер экспрессии VDR, усиливающейся по мере роста и созревания фолликула.
Yao et al. также подтвердили, что уровни мРНК и белка VDR в гранулёзных клетках коз значительно возрастали с увеличением диаметра фолликула (P < 0,05). Эти данные подтверждают, что экспрессия VDR в фолликулах зависит от стадии их развития и возрастает по мере созревания.
Xu et al. также показали, что в фолликулах, культивируемых in vitro, уровни мРНК VDR были ниже по сравнению с фолликулами, развивающимися in vivo, однако после добавления витамина D3 восстанавливались до уровней in vivo. В свою очередь, Grzesiak et al. обнаружили максимальную экспрессию мРНК VDR в малых антральных фолликулах свиней, культивируемых in vitro, с последующим постепенным снижением экспрессии по мере развития фолликулов. Вероятно, это связано с истощением витамина D3 в условиях in vitro-культивирования.
Исследования показывают, что концентрация витамина D3 способна динамически регулировать количество гетеродимерных комплексов VDR/RXR в участках связывания VDR, тем самым влияя на экспрессию самого рецептора. Однако точные молекулярные механизмы этого процесса пока остаются неясными.
В исследовании фолликулов макак-резусов, культивируемых in vitro, Xu et al. показали, что уровень мРНК CYP2R1 был выше в малых антральных фолликулах по сравнению с преантральными (P < 0,05), тогда как уровень мРНК CYP27B1 существенно не изменялся. В то же время Grzesiak в исследовании фолликулов свиней обнаружил более высокие уровни мРНК и белка CYP27B1 в средних антральных фолликулах по сравнению с малыми антральными фолликулами (мРНК: увеличение в 1,55 раза, P = 0,042; белок: в 2,49 раза, P = 0,005). Кроме того, уровень мРНК CYP24A1 также был выше в средних антральных фолликулах (в 1,96 раза; P = 0,042), тогда как различий по уровню белка между стадиями развития фолликулов не выявлено.
Эти различия могут быть связаны с межвидовыми особенностями и различиями стадий развития анализируемых фолликулов. В совокупности данные указывают на усиление экспрессии ферментов синтеза витамина D3 по мере созревания фолликулов. Кроме того, добавление витамина D3 в культуральную среду приводило к значительному повышению уровня мРНК CYP2R1 в преантральных фолликулах через две недели, что позволяет предположить наличие положительной обратной связи, усиливающей синтез витамина D3 в преантральных фолликулах.
Однако реализация эффектов витамина D3 также зависит от распределения его рецептора — рецептора витамина D (VDR). В присутствии лиганда VDR образует гетеродимерный комплекс с рецептором ретиноидов X (RXR), формируя комплекс VDR/RXR. Этот комплекс связывается с элементами ответа на витамин D в промоторных участках генов-мишеней и регулирует экспрессию генов через каскады сигнальных путей, обеспечивая биологические эффекты.
В 1983 году Dokoh et al. впервые обнаружили экспрессию VDR в яичниках млекопитающих и птиц. Позднее иммуннофлуоресцентное окрашивание VDR было выявлено в ооцитах примордиальных фолликулов у рыб, коз и макак-резусов. В отличие от этого, в первичных и вторичных фолликулах крыс и коз экспрессия VDR преимущественно наблюдалась в гранулёзных клетках (GCs) и тека-клетках (TCs).
В исследованиях ткани яичников макак-резусов Xu et al. использовали иммуногистохимическое окрашивание для оценки экспрессии белка VDR. Было показано, что VDR экспрессируется на всех стадиях развития ооцита. Хотя экспрессия VDR также выявлялась в прегранулёзных клетках примордиальных фолликулов, она была менее выраженной. В гранулёзных клетках первичных фолликулов отмечалось лишь минимальное окрашивание VDR. Однако по мере перехода фолликулов к стадиям вторичных, малых антральных и крупных антральных фолликулов интенсивность окрашивания гранулёзных клеток постепенно увеличивалась. Это указывает на стадийно-зависимый характер экспрессии VDR, усиливающейся по мере роста и созревания фолликула.
Yao et al. также подтвердили, что уровни мРНК и белка VDR в гранулёзных клетках коз значительно возрастали с увеличением диаметра фолликула (P < 0,05). Эти данные подтверждают, что экспрессия VDR в фолликулах зависит от стадии их развития и возрастает по мере созревания.
Xu et al. также показали, что в фолликулах, культивируемых in vitro, уровни мРНК VDR были ниже по сравнению с фолликулами, развивающимися in vivo, однако после добавления витамина D3 восстанавливались до уровней in vivo. В свою очередь, Grzesiak et al. обнаружили максимальную экспрессию мРНК VDR в малых антральных фолликулах свиней, культивируемых in vitro, с последующим постепенным снижением экспрессии по мере развития фолликулов. Вероятно, это связано с истощением витамина D3 в условиях in vitro-культивирования.
Исследования показывают, что концентрация витамина D3 способна динамически регулировать количество гетеродимерных комплексов VDR/RXR в участках связывания VDR, тем самым влияя на экспрессию самого рецептора. Однако точные молекулярные механизмы этого процесса пока остаются неясными.
Витамин D3 и развитие фолликулов
Ранее проведённые исследования указывают на возможное участие витамина D3 в фолликулогенезе. В контрольном эксперименте с использованием мышей с нокаутом гена CYP27B1 Dicken et al. показали, что дефицит витамина D3 в рационе приводил к задержке развития яичников и удлинению эстрального цикла. Однако после добавления витамина D3 в рацион эстральный цикл нормализовался.
Xu и соавт. изучали влияние витамина D3 на развитие фолликулов с использованием трёхмерной модели культивирования фолликулов макак-резусов. Результаты показали, что после 5 недель культивирования in vitro как низкие (25 пг/мл), так и высокие (100 пг/мл) дозы витамина D3 приводили к увеличению диаметра ооцитов в антральных фолликулах по сравнению с контрольной группой (P < 0,05). Кроме того, высокая доза витамина D3 увеличивала долю растущих фолликулов, что указывает на его стимулирующее влияние на рост антральных фолликулов и непосредственное участие в регуляции фолликулярного развития. В данном разделе с учётом современных исследований рассматриваются возможные механизмы этих эффектов.
Xu и соавт. изучали влияние витамина D3 на развитие фолликулов с использованием трёхмерной модели культивирования фолликулов макак-резусов. Результаты показали, что после 5 недель культивирования in vitro как низкие (25 пг/мл), так и высокие (100 пг/мл) дозы витамина D3 приводили к увеличению диаметра ооцитов в антральных фолликулах по сравнению с контрольной группой (P < 0,05). Кроме того, высокая доза витамина D3 увеличивала долю растущих фолликулов, что указывает на его стимулирующее влияние на рост антральных фолликулов и непосредственное участие в регуляции фолликулярного развития. В данном разделе с учётом современных исследований рассматриваются возможные механизмы этих эффектов.

Ооцит
Клеточный цикл растущих ооцитов останавливается на стадии профазы I мейоза и возобновляется лишь за несколько часов до овуляции. В этот период ооциты накапливают большое количество транскриптов и белков, необходимых для раннего эмбрионального развития.
Этот процесс реализуется через сигнальный путь C-типа натрийуретического пептида (NPPC). NPPC, секретируемый пристеночными гранулёзными клетками (MGC), связывается со своим рецептором NPR2, инициируя синтез циклического гуанозинмонофосфата (cGMP). Далее cGMP через щелевые контакты поступает в ооцит, что приводит к повышению уровня циклического аденозинмонофосфата (cAMP) и поддержанию мейотического ареста ооцита (рис. 1).
Этот процесс реализуется через сигнальный путь C-типа натрийуретического пептида (NPPC). NPPC, секретируемый пристеночными гранулёзными клетками (MGC), связывается со своим рецептором NPR2, инициируя синтез циклического гуанозинмонофосфата (cGMP). Далее cGMP через щелевые контакты поступает в ооцит, что приводит к повышению уровня циклического аденозинмонофосфата (cAMP) и поддержанию мейотического ареста ооцита (рис. 1).
Трансформирующий фактор роста β (TGF-β) — семейство факторов роста, тесно связанное с белками Smad. После связывания с рецептором TGFR активируется Smad2/3. Активированные Smad2/3 образуют гетеромерные комплексы со Smad4 и транслоцируются в ядро, где связываются с промоторной областью NPPC, значительно повышая уровень NPPC в культивируемых пристеночных гранулёзных клетках (рис. 1).
Рис.1
(AMH — антимюллеров гормон; FSH — фолликулостимулирующий гормон. Красные стрелки обозначают стимуляцию, синие — ингибирование.)
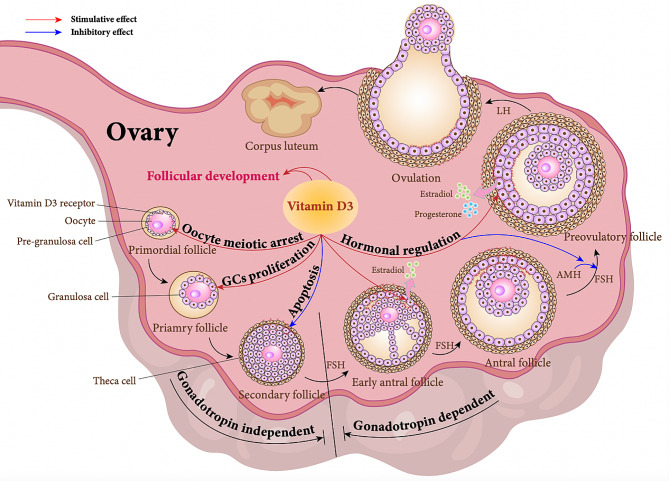
Роль витамина D3 в фолликулогенезе
В зависимости от стадии развития выделяют примордиальные, первичные, вторичные, антральные и зрелые фолликулы. На этапе перехода вторичных фолликулов в антральные начинается экспрессия гормональных рецепторов, и фолликулы переходят в гонадотропин-зависимую стадию развития.
Витамин D3 способствует развитию фолликулов за счёт стимуляции мейоза ооцитов, пролиферации гранулёзных клеток, усиления секреции эстрогенов и прогестерона фолликулярными клетками, ослабления ингибирующего влияния АМГ на ФСГ, а также снижения клеточного апоптоза.
Corduk и соавт. провели хорошо спланированное рандомизированное контролируемое исследование с участием 24 мышей. Животные экспериментальной группы получали инъекции витамина D3 (0,05 мкг/кг один раз в два дня) в течение 8 недель. По сравнению с контрольной группой после введения витамина D3 иммуногистохимическое окрашивание TGF-β1 в яичниках взрослых крыс было отрицательным, что позволяет предположить, что витамин D3 может способствовать развитию ооцитов за счёт восстановления их мейотического статуса посредством снижения уровня TGF-β1.
При этом в яичниках новорождённых крыс значимого снижения экспрессии TGF-β1 выявлено не было, что, вероятно, связано с незрелостью системы VDR в этот период развития. Кроме того, Han et al. показали на первичных клетках лёгочной ткани трансгенных мышей с гиперэкспрессией TGF-β1, что добавление витамина D3 снижало экспрессию TGF-β1 и фосфорилированного Smad-2/3. Аналогично Wang et al. продемонстрировали, что витамин D3 уменьшал выраженность почечного фиброза у крыс с хронической болезнью почек (ХБП) за счёт повышения экспрессии VDR и ингибирования сигнального пути TGF-β1/Smad3.
Эти данные позволяют предположить, что витамин D3 способен подавлять сигнальный путь TGF-β1/Smad3, потенциально снижая уровень NPPC, преодолевая мейотический арест ооцитов и тем самым способствуя развитию фолликулов.
После связывания NPPC со своим рецептором образующийся cGMP должен проходить через белки щелевых контактов, чтобы попасть в ооцит и поддерживать его мейотический арест. Коннексин 43 (Cx43) и коннексин 37 (Cx37) являются ключевыми белками щелевых контактов при развитии фолликулов и играют важную роль в поддержании мейотического ареста.
Richard et al. использовали коннексин-миметические пептиды (CMPs) для нарушения гетеромерных щелевых контактов. Добавление Cx43 CMP в культуральную среду значительно увеличивало частоту возобновления мейоза ооцитов в комплексах «кумулюс–ооцит» (COCs). В отличие от этого, Cx37 CMP не оказывал эффекта при добавлении в среду, однако его микроинъекция в периооцитарное пространство рядом с поверхностью ооцита приводила к снятию блока мейоза. Эти результаты согласуются с ранее полученными данными о том, что Cx43 локализуется преимущественно в клетках кумулюса, тогда как Cx37 — на поверхности ооцита.
Кроме того, Ackert et al. показали, что у мышей с трансплантированными яичниками, лишёнными Cx43, в цитоплазме ооцитов и гранулёзных клеток формировались вакуоли, что сопровождалось задержкой роста ооцитов и нарушением завершения финальных мейотических делений и оплодотворения. Также было показано, что обработка ооцитов крупного рогатого скота Cx37 в концентрации 25 мкг/мл перед экстракорпоральным оплодотворением (IVF) значительно улучшала ядерное созревание и развитие эмбрионов по сравнению с контрольной группой.
Все эти данные свидетельствуют о критической роли Cx43 и Cx37 в созревании ооцитов.
Ранее было показано, что витамин D3 способен повышать экспрессию Cx43 в звёздчатых клетках печени крыс, усиливая межклеточную коммуникацию. На основании этих данных Lee et al. установили, что в первичной культуре гранулёзных клеток крыс витамин D3 (0,1 мкМ) способен нивелировать ингибирующее действие высоких концентраций тестостерона (1 мкг/мл) на экспрессию Cx43 в гранулёзных клетках, тем самым способствуя развитию фолликулов.
Витамин D3 способствует развитию фолликулов за счёт стимуляции мейоза ооцитов, пролиферации гранулёзных клеток, усиления секреции эстрогенов и прогестерона фолликулярными клетками, ослабления ингибирующего влияния АМГ на ФСГ, а также снижения клеточного апоптоза.
Corduk и соавт. провели хорошо спланированное рандомизированное контролируемое исследование с участием 24 мышей. Животные экспериментальной группы получали инъекции витамина D3 (0,05 мкг/кг один раз в два дня) в течение 8 недель. По сравнению с контрольной группой после введения витамина D3 иммуногистохимическое окрашивание TGF-β1 в яичниках взрослых крыс было отрицательным, что позволяет предположить, что витамин D3 может способствовать развитию ооцитов за счёт восстановления их мейотического статуса посредством снижения уровня TGF-β1.
При этом в яичниках новорождённых крыс значимого снижения экспрессии TGF-β1 выявлено не было, что, вероятно, связано с незрелостью системы VDR в этот период развития. Кроме того, Han et al. показали на первичных клетках лёгочной ткани трансгенных мышей с гиперэкспрессией TGF-β1, что добавление витамина D3 снижало экспрессию TGF-β1 и фосфорилированного Smad-2/3. Аналогично Wang et al. продемонстрировали, что витамин D3 уменьшал выраженность почечного фиброза у крыс с хронической болезнью почек (ХБП) за счёт повышения экспрессии VDR и ингибирования сигнального пути TGF-β1/Smad3.
Эти данные позволяют предположить, что витамин D3 способен подавлять сигнальный путь TGF-β1/Smad3, потенциально снижая уровень NPPC, преодолевая мейотический арест ооцитов и тем самым способствуя развитию фолликулов.
После связывания NPPC со своим рецептором образующийся cGMP должен проходить через белки щелевых контактов, чтобы попасть в ооцит и поддерживать его мейотический арест. Коннексин 43 (Cx43) и коннексин 37 (Cx37) являются ключевыми белками щелевых контактов при развитии фолликулов и играют важную роль в поддержании мейотического ареста.
Richard et al. использовали коннексин-миметические пептиды (CMPs) для нарушения гетеромерных щелевых контактов. Добавление Cx43 CMP в культуральную среду значительно увеличивало частоту возобновления мейоза ооцитов в комплексах «кумулюс–ооцит» (COCs). В отличие от этого, Cx37 CMP не оказывал эффекта при добавлении в среду, однако его микроинъекция в периооцитарное пространство рядом с поверхностью ооцита приводила к снятию блока мейоза. Эти результаты согласуются с ранее полученными данными о том, что Cx43 локализуется преимущественно в клетках кумулюса, тогда как Cx37 — на поверхности ооцита.
Кроме того, Ackert et al. показали, что у мышей с трансплантированными яичниками, лишёнными Cx43, в цитоплазме ооцитов и гранулёзных клеток формировались вакуоли, что сопровождалось задержкой роста ооцитов и нарушением завершения финальных мейотических делений и оплодотворения. Также было показано, что обработка ооцитов крупного рогатого скота Cx37 в концентрации 25 мкг/мл перед экстракорпоральным оплодотворением (IVF) значительно улучшала ядерное созревание и развитие эмбрионов по сравнению с контрольной группой.
Все эти данные свидетельствуют о критической роли Cx43 и Cx37 в созревании ооцитов.
Ранее было показано, что витамин D3 способен повышать экспрессию Cx43 в звёздчатых клетках печени крыс, усиливая межклеточную коммуникацию. На основании этих данных Lee et al. установили, что в первичной культуре гранулёзных клеток крыс витамин D3 (0,1 мкМ) способен нивелировать ингибирующее действие высоких концентраций тестостерона (1 мкг/мл) на экспрессию Cx43 в гранулёзных клетках, тем самым способствуя развитию фолликулов.
Пролиферация гранулёзных клеток (GCs)
В процессе развития фолликула гранулёзные клетки обеспечивают ооцит необходимой структурной поддержкой и формируют микроокружение, необходимое для его созревания. В исследованиях in vitro показано, что как низкие (10 нМ), так и высокие (100 нМ) концентрации витамина D3 способны стимулировать пролиферацию гранулёзных клеток в фолликулах кур. Позднее было подтверждено, что витамин D3 дозозависимо усиливает пролиферацию лютеинизированных гранулёзных клеток коз. Регуляция пролиферации гранулёзных клеток витамином D3 реализуется через несколько механизмов.
Одним из ключевых механизмов является регуляция клеточного цикла. Клеточный цикл контролируется циклинами, циклин-зависимыми киназами (CDKs) и ингибиторами циклин-зависимых киназ (CKIs). В исследованиях in vitro показано, что витамин D3 в концентрации 10 нМ стимулирует пролиферацию гранулёзных клеток в фолликулах коз диаметром 2–5 мм (P < 0,05).
После 48 часов воздействия витамина D3 уровень мРНК Cyclin-dependent kinase 4 (CDK4) и Cyclin D1 в гранулёзных клетках значительно повышался, тогда как экспрессия ингибиторов клеточного цикла, включая P21, снижалась. Кроме того, по данным проточной цитометрии увеличивалась доля клеток в S-фазе и уменьшалась доля клеток в фазе G0/G1.
Ранее было показано, что активация комплекса Cyclin D1-CDK4 необходима для прохождения клеткой контрольной точки G1/S. В дальнейшем при подавлении экспрессии VDR в гранулёзных клетках были получены противоположные результаты, что дополнительно подтвердило роль витамина D3 в регуляции клеточного цикла.
Таким образом, витамин D3 усиливает экспрессию CDK4 и Cyclin D1 и одновременно подавляет экспрессию P21, что приводит к активации pRb, высвобождению транскрипционного фактора E2F и переходу клеток из фазы G0/G1 в S-фазу. Эти данные указывают на то, что витамин D3 способен опосредованно влиять на развитие фолликулов через стимуляцию пролиферации гранулёзных клеток.
Однако при воздействии высокой концентрации витамина D3 (100 нМ) в течение 48 часов наблюдались противоположные эффекты, аналогичные ранее описанным в опухолевых клетках. В то же время в культуре фолликулов кур добавление витамина D3 в концентрации 100 нМ в течение 24 часов, напротив, стимулировало пролиферацию гранулёзных клеток. Эти различия могут быть связаны с меньшей продолжительностью воздействия витамина D3, межвидовыми особенностями, а также взаимодействием гранулёзных клеток с другими клетками внутри культивируемого фолликула.
Поэтому для уточнения влияния высоких доз витамина D3 на развитие фолликулов и пролиферацию гранулёзных клеток необходимы дополнительные исследования.
Одним из ключевых механизмов является регуляция клеточного цикла. Клеточный цикл контролируется циклинами, циклин-зависимыми киназами (CDKs) и ингибиторами циклин-зависимых киназ (CKIs). В исследованиях in vitro показано, что витамин D3 в концентрации 10 нМ стимулирует пролиферацию гранулёзных клеток в фолликулах коз диаметром 2–5 мм (P < 0,05).
После 48 часов воздействия витамина D3 уровень мРНК Cyclin-dependent kinase 4 (CDK4) и Cyclin D1 в гранулёзных клетках значительно повышался, тогда как экспрессия ингибиторов клеточного цикла, включая P21, снижалась. Кроме того, по данным проточной цитометрии увеличивалась доля клеток в S-фазе и уменьшалась доля клеток в фазе G0/G1.
Ранее было показано, что активация комплекса Cyclin D1-CDK4 необходима для прохождения клеткой контрольной точки G1/S. В дальнейшем при подавлении экспрессии VDR в гранулёзных клетках были получены противоположные результаты, что дополнительно подтвердило роль витамина D3 в регуляции клеточного цикла.
Таким образом, витамин D3 усиливает экспрессию CDK4 и Cyclin D1 и одновременно подавляет экспрессию P21, что приводит к активации pRb, высвобождению транскрипционного фактора E2F и переходу клеток из фазы G0/G1 в S-фазу. Эти данные указывают на то, что витамин D3 способен опосредованно влиять на развитие фолликулов через стимуляцию пролиферации гранулёзных клеток.
Однако при воздействии высокой концентрации витамина D3 (100 нМ) в течение 48 часов наблюдались противоположные эффекты, аналогичные ранее описанным в опухолевых клетках. В то же время в культуре фолликулов кур добавление витамина D3 в концентрации 100 нМ в течение 24 часов, напротив, стимулировало пролиферацию гранулёзных клеток. Эти различия могут быть связаны с меньшей продолжительностью воздействия витамина D3, межвидовыми особенностями, а также взаимодействием гранулёзных клеток с другими клетками внутри культивируемого фолликула.
Поэтому для уточнения влияния высоких доз витамина D3 на развитие фолликулов и пролиферацию гранулёзных клеток необходимы дополнительные исследования.
Гормональная регуляция
Рост и развитие фолликулов регулируются различными гормонами и факторами роста, включая фолликулостимулирующий гормон (FSH), лютеинизирующий гормон (LH), эпидермальный фактор роста (EGF), инсулиноподобный фактор роста (IGF), а также ингибирующие факторы, в частности антимюллеров гормон (AMH).
Витамин D3 способен модулировать активность ряда гормонов, необходимых для роста фолликулов, тем самым влияя на процессы фолликулогенеза.
Витамин D3 способен модулировать активность ряда гормонов, необходимых для роста фолликулов, тем самым влияя на процессы фолликулогенеза.

АМГ (антимюллеров гормон)
В исследовании с участием 351 здоровой женщины репродуктивного возраста было показано, что как общий, так и свободный уровень витамина D3 в сыворотке крови обратно коррелировал с уровнем антимюллерова гормона (АМГ).
Антимюллеров гормон (АМГ) относится к суперсемейству TGF-β и регулируется генами семейства Smad. Его экспрессия впервые появляется в гранулёзных клетках преантральных и ранних антральных фолликулов. Максимальная экспрессия гена АМГ и его белка наблюдается в фолликулах диаметром около 8 мм, после чего по мере увеличения диаметра фолликула резко снижается.
Рецептор АМГ II типа (AMHR-II) экспрессируется в гранулёзных и тека-клетках преантральных и малых антральных фолликулов, тогда как в крупных антральных и преовуляторных фолликулах его экспрессия сохраняется преимущественно в тека-клетках.
АМГ является одним из ключевых регуляторов ранних стадий фолликулогенеза. Он подавляет активацию примордиальных фолликулов и тормозит их развитие за счёт ингибирования апоптоза ооцитов. Однако на гормонозависимой стадии развития фолликулов АМГ снижает чувствительность растущих фолликулов к ФСГ посредством подавления экспрессии рецепторов ФСГ, тем самым участвуя в регуляции рекрутирования фолликулов и отбора доминантного фолликула.
В исследовании фолликулярной жидкости 54 пациенток программы ЭКО показана отрицательная корреляция между уровнем витамина D3 и экспрессией мРНК AMH и AMHR-II в кумулюсных гранулёзных клетках малых антральных фолликулов (P < 0,05), тогда как в пристеночных гранулёзных клетках значимых различий не выявлено.
После обработки изолированных кумулюсных гранулёзных клеток витамином D3 (50 нМ) в течение 24 часов уровень AMHR-II снижался на 36% по сравнению с контролем (P < 0,05), при этом статистически значимых изменений уровня белка AMH не наблюдалось.
Кроме того, комбинация витамина D3 и рекомбинантного AMH вызывала более выраженное снижение ядерного фосфорилирования Smad 1/5/8 в гранулёзных клетках по сравнению с воздействием одного AMH (P < 0,0001). Это позволяет предположить, что витамин D3 способен ослаблять действие AMH за счёт уменьшения фосфорилирования и ядерной локализации белков семейства Smad, а также подавления экспрессии AMHR-II, тем самым снижая ингибирующее влияние AMH на гранулёзные клетки и способствуя созреванию фолликулов.
Однако в клетках рака предстательной железы человека было показано, что в промоторной области гена AMH присутствует последовательность, сходная с элементом ответа на витамин D, и витамин D3 способен усиливать экспрессию AMH через функциональный VDRE, связанный с VDR. Вероятно, такие различия связаны с типом клеток и межвидовыми особенностями.
Недавний систематический обзор и метаанализ показали, что влияние витамина D3 на уровень AMH зависит от овуляторного статуса пациенток. После приёма витамина D3 уровень AMH значительно снижался у пациенток с ановуляторным СПКЯ (SMD −0,53; 95% ДИ от −0,91 до −0,15; p < 0,007), тогда как у овулирующих женщин без СПКЯ он, напротив, повышался (SMD 0,49; 95% ДИ 0,17–0,80; p = 0,003).
Эти данные указывают на возможный двунаправленный характер регуляции AMH витамином D3. В связи с этим необходимы дополнительные клинические исследования с контролем таких факторов, как овуляторный статус, сезон, питание и индекс массы тела. Также требует дальнейшего изучения вопрос о необходимости индивидуального подбора доз витамина D в зависимости от исходного уровня витамина D у пациенток.
Антимюллеров гормон (АМГ) относится к суперсемейству TGF-β и регулируется генами семейства Smad. Его экспрессия впервые появляется в гранулёзных клетках преантральных и ранних антральных фолликулов. Максимальная экспрессия гена АМГ и его белка наблюдается в фолликулах диаметром около 8 мм, после чего по мере увеличения диаметра фолликула резко снижается.
Рецептор АМГ II типа (AMHR-II) экспрессируется в гранулёзных и тека-клетках преантральных и малых антральных фолликулов, тогда как в крупных антральных и преовуляторных фолликулах его экспрессия сохраняется преимущественно в тека-клетках.
АМГ является одним из ключевых регуляторов ранних стадий фолликулогенеза. Он подавляет активацию примордиальных фолликулов и тормозит их развитие за счёт ингибирования апоптоза ооцитов. Однако на гормонозависимой стадии развития фолликулов АМГ снижает чувствительность растущих фолликулов к ФСГ посредством подавления экспрессии рецепторов ФСГ, тем самым участвуя в регуляции рекрутирования фолликулов и отбора доминантного фолликула.
В исследовании фолликулярной жидкости 54 пациенток программы ЭКО показана отрицательная корреляция между уровнем витамина D3 и экспрессией мРНК AMH и AMHR-II в кумулюсных гранулёзных клетках малых антральных фолликулов (P < 0,05), тогда как в пристеночных гранулёзных клетках значимых различий не выявлено.
После обработки изолированных кумулюсных гранулёзных клеток витамином D3 (50 нМ) в течение 24 часов уровень AMHR-II снижался на 36% по сравнению с контролем (P < 0,05), при этом статистически значимых изменений уровня белка AMH не наблюдалось.
Кроме того, комбинация витамина D3 и рекомбинантного AMH вызывала более выраженное снижение ядерного фосфорилирования Smad 1/5/8 в гранулёзных клетках по сравнению с воздействием одного AMH (P < 0,0001). Это позволяет предположить, что витамин D3 способен ослаблять действие AMH за счёт уменьшения фосфорилирования и ядерной локализации белков семейства Smad, а также подавления экспрессии AMHR-II, тем самым снижая ингибирующее влияние AMH на гранулёзные клетки и способствуя созреванию фолликулов.
Однако в клетках рака предстательной железы человека было показано, что в промоторной области гена AMH присутствует последовательность, сходная с элементом ответа на витамин D, и витамин D3 способен усиливать экспрессию AMH через функциональный VDRE, связанный с VDR. Вероятно, такие различия связаны с типом клеток и межвидовыми особенностями.
Недавний систематический обзор и метаанализ показали, что влияние витамина D3 на уровень AMH зависит от овуляторного статуса пациенток. После приёма витамина D3 уровень AMH значительно снижался у пациенток с ановуляторным СПКЯ (SMD −0,53; 95% ДИ от −0,91 до −0,15; p < 0,007), тогда как у овулирующих женщин без СПКЯ он, напротив, повышался (SMD 0,49; 95% ДИ 0,17–0,80; p = 0,003).
Эти данные указывают на возможный двунаправленный характер регуляции AMH витамином D3. В связи с этим необходимы дополнительные клинические исследования с контролем таких факторов, как овуляторный статус, сезон, питание и индекс массы тела. Также требует дальнейшего изучения вопрос о необходимости индивидуального подбора доз витамина D в зависимости от исходного уровня витамина D у пациенток.
Эстрадиол
В ретроспективном исследовании с участием 89 женщин репродуктивного возраста показано, что при низком уровне витамина D в сыворотке крови (<30 нг/мл) средние концентрации эстрадиола (E2) в течение менструального цикла были ниже.
Кроме того, в культуре ткани яичника человека добавление витамина D3 (50 нМ) увеличивало синтез эстрадиола на 9% (p < 0,02), а совместное применение витамина D3 и инсулина — на 60% (p < 0,005), что указывает на их синергичное действие в стимуляции продукции эстрадиола.
Синтез E2 необходим для нормального развития фолликулов и овуляции и осуществляется в гранулёзных клетках (рис. 2). Ранее было показано, что витамин D3 усиливает превращение андростендиона в эстрон в фибробластах кожи человека, и аналогичный механизм, вероятно, реализуется и в гранулёзных клетках.
Позднее в культуре гранулёзных клеток свиней было установлено, что после 24 часов воздействия витамина D3 (100 нМ) значительно повышалась экспрессия генов, связанных с синтезом эстрогенов, включая CYP17A1, HSD17B1 и CYP19A1. При этом увеличение уровней белков CYP17A1 и CYP19A1 не достигало статистической значимости, что может быть связано с концентрацией витамина D3 и продолжительностью воздействия.
Недавно показано, что у кур-несушек, получавших витамин D3 в дозировках 10 и 100 мкг/кг в течение 4 недель, уровни E2 и прогестерона (P4) в сыворотке крови значительно повышались. Транскриптомный анализ ткани яичников продемонстрировал изменение экспрессии генов стероидогенеза под влиянием витамина D3.
По сравнению с контрольной группой экспрессия мРНК HSD17B1 — ключевого фермента синтеза эстрогенов — была выше при низких дозах витамина D3 и ниже при высоких. Это свидетельствует о том, что адекватный уровень витамина D3 способствует продукции эстрадиола в гранулёзных клетках через усиление экспрессии HSD17B1.
HSD17B1 обеспечивает превращение тестостерона в 17β-эстрадиол в гранулёзных клетках, способствуя созреванию фолликулов. Однако избыток тестостерона может подавлять активность этого фермента.
В модели гранулёзных клеток крыс с индуцированным гиперандрогенным состоянием показано, что витамин D3 в концентрации 0,1 мкМ значительно ослаблял ингибирующее влияние высоких доз тестостерона (1 мкг/мл) на активность ароматазы, вероятно за счёт усиления тирозинового фосфорилирования ароматазы.
Кроме того, в культуре ткани яичника человека добавление витамина D3 (50 нМ) увеличивало синтез эстрадиола на 9% (p < 0,02), а совместное применение витамина D3 и инсулина — на 60% (p < 0,005), что указывает на их синергичное действие в стимуляции продукции эстрадиола.
Синтез E2 необходим для нормального развития фолликулов и овуляции и осуществляется в гранулёзных клетках (рис. 2). Ранее было показано, что витамин D3 усиливает превращение андростендиона в эстрон в фибробластах кожи человека, и аналогичный механизм, вероятно, реализуется и в гранулёзных клетках.
Позднее в культуре гранулёзных клеток свиней было установлено, что после 24 часов воздействия витамина D3 (100 нМ) значительно повышалась экспрессия генов, связанных с синтезом эстрогенов, включая CYP17A1, HSD17B1 и CYP19A1. При этом увеличение уровней белков CYP17A1 и CYP19A1 не достигало статистической значимости, что может быть связано с концентрацией витамина D3 и продолжительностью воздействия.
Недавно показано, что у кур-несушек, получавших витамин D3 в дозировках 10 и 100 мкг/кг в течение 4 недель, уровни E2 и прогестерона (P4) в сыворотке крови значительно повышались. Транскриптомный анализ ткани яичников продемонстрировал изменение экспрессии генов стероидогенеза под влиянием витамина D3.
По сравнению с контрольной группой экспрессия мРНК HSD17B1 — ключевого фермента синтеза эстрогенов — была выше при низких дозах витамина D3 и ниже при высоких. Это свидетельствует о том, что адекватный уровень витамина D3 способствует продукции эстрадиола в гранулёзных клетках через усиление экспрессии HSD17B1.
HSD17B1 обеспечивает превращение тестостерона в 17β-эстрадиол в гранулёзных клетках, способствуя созреванию фолликулов. Однако избыток тестостерона может подавлять активность этого фермента.
В модели гранулёзных клеток крыс с индуцированным гиперандрогенным состоянием показано, что витамин D3 в концентрации 0,1 мкМ значительно ослаблял ингибирующее влияние высоких доз тестостерона (1 мкг/мл) на активность ароматазы, вероятно за счёт усиления тирозинового фосфорилирования ароматазы.
Пути синтеза эстрогенов и прогестерона. Синтез эстрогенов и прогестерона происходит в фолликулярных клетках. Гены CYP11A1, CYP17, 3β-HSD, 17β-HSD и P450arom кодируют ферменты стероидогенеза и совместно регулируют синтез эстрогенов и прогестерона. (P450arom кодирует ароматазу — ключевой лимитирующий фермент синтеза эстрогенов.)
Рис.2
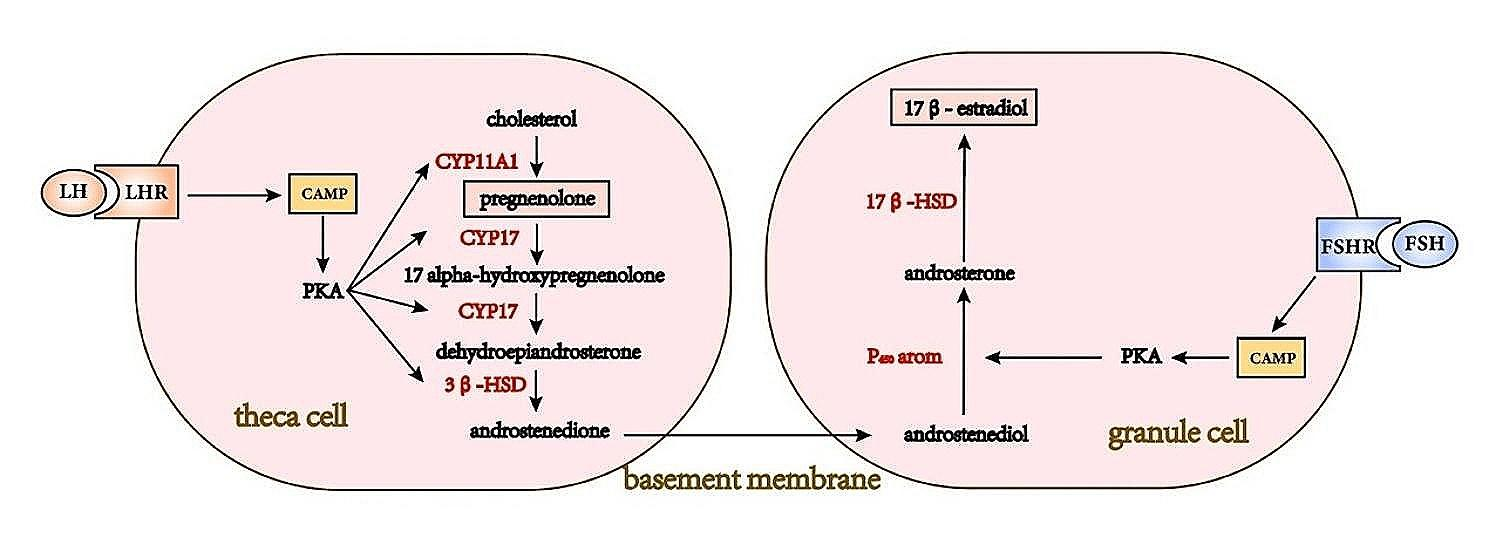
Прогестерон
У мышей с дефицитом 25-гидроксивитамин D1α-гидроксилазы наблюдалось снижение уровней эстрогенов и прогестерона в сыворотке крови, что позволяет предположить связь дефицита витамина D3 со снижением уровня прогестерона (P4).
Прогестерон вырабатывается гранулёзными и тека-клетками фолликулов и необходим для нормального развития фолликулов. Синтез P4 представляет собой сложный процесс, регулируемый steroidogenic acute regulatory protein (StAR) и 3β-гидроксистероиддегидрогеназой (3β-HSD) (рис. 2).
В исследовании гранулёзных клеток коз показано, что воздействие витамина D3 (10 нМ) или FSH (10 нг/мл) в течение 48 часов по отдельности значимо повышало продукцию P4 (P < 0,05), однако витамин D3 не усиливал стимулирующее действие FSH на синтез прогестерона.
Кроме того, по сравнению с контрольной группой в гранулёзных клетках, обработанных витамином D3, наблюдалось значительное повышение экспрессии мРНК 3β-HSD и StAR. Это свидетельствует о том, что витамин D3 стимулирует синтез прогестерона за счёт усиления экспрессии генов, связанных со стероидогенезом, тем самым способствуя развитию фолликулов (рис. 3).
Эти данные согласуются с результатами предыдущих исследований, в которых показано, что добавление витамина D3 (50 нМ) увеличивало синтез и секрецию P4 в кумулюсных гранулёзных клетках, сопровождаясь повышением уровня мРНК 3β-HSD и активности фермента 3β-HSD.
Это позволяет предположить, что стимулирующее влияние витамина D3 на синтез прогестерона может включать механизм положительной обратной связи, требующий дальнейшего изучения.
Прогестерон вырабатывается гранулёзными и тека-клетками фолликулов и необходим для нормального развития фолликулов. Синтез P4 представляет собой сложный процесс, регулируемый steroidogenic acute regulatory protein (StAR) и 3β-гидроксистероиддегидрогеназой (3β-HSD) (рис. 2).
В исследовании гранулёзных клеток коз показано, что воздействие витамина D3 (10 нМ) или FSH (10 нг/мл) в течение 48 часов по отдельности значимо повышало продукцию P4 (P < 0,05), однако витамин D3 не усиливал стимулирующее действие FSH на синтез прогестерона.
Кроме того, по сравнению с контрольной группой в гранулёзных клетках, обработанных витамином D3, наблюдалось значительное повышение экспрессии мРНК 3β-HSD и StAR. Это свидетельствует о том, что витамин D3 стимулирует синтез прогестерона за счёт усиления экспрессии генов, связанных со стероидогенезом, тем самым способствуя развитию фолликулов (рис. 3).
Эти данные согласуются с результатами предыдущих исследований, в которых показано, что добавление витамина D3 (50 нМ) увеличивало синтез и секрецию P4 в кумулюсных гранулёзных клетках, сопровождаясь повышением уровня мРНК 3β-HSD и активности фермента 3β-HSD.
Это позволяет предположить, что стимулирующее влияние витамина D3 на синтез прогестерона может включать механизм положительной обратной связи, требующий дальнейшего изучения.
Молекулярные механизмы влияния витамина D3 на развитие фолликулов. TGF-β1 связывается со своим рецептором, активируя Smad2/3, которые затем образуют гетеромерный комплекс со Smad4 и транслоцируются в ядро клетки. В ядре этот комплекс связывается с промоторной областью NPPC, стимулируя синтез NPPC. В свою очередь NPPC активирует синтез cGMP, который через коннексины CX43 и CX37 поступает в ооцит и поддерживает его мейотический арест.
Витамин D3 способствует возобновлению мейоза ооцитов за счёт ингибирования сигнального пути TGF-β1. Кроме того, витамин D3 способен ослаблять ингибирующее влияние избытка тестостерона на CX43. LH подавляет сигнальный путь TGF-β1, тогда как FSH, напротив, активирует его.
Витамин D3 стимулирует пролиферацию гранулёзных клеток посредством повышения экспрессии мРНК CDK4 и CyclinD1 и подавления экспрессии мРНК P21. Он также усиливает секрецию E2 и P4 гранулёзными клетками за счёт стимуляции экспрессии ферментов стероидогенеза, тем самым способствуя развитию фолликулов.
Кроме того, витамин D3 снижает синтез мРНК AMHR-II посредством ингибирования фосфорилирования SMAD 1/5/8. За счёт повышения уровней SOD и CAT витамин D3 уменьшает образование ROS, оказывая противовоспалительное действие и снижая негативное влияние оксидативного стресса на развитие фолликулов.
Недавно было показано, что добавление витамина D3 в рацион кур-несушек приводило к значительному повышению уровня P4 в сыворотке крови при одновременном снижении уровня общего холестерина.
В дальнейшем установлено, что после 24 часов культивирования фолликулов кур in vitro с витамином D3 (10 нМ и 100 нМ) уровни P4 в гранулёзных и тека-клетках значительно повышались. Дополнительный ПЦР-анализ показал, что витамин D3 в концентрации 10 нМ существенно повышал уровень мРНК CYP11A1.
Фермент, кодируемый CYP11A1, обеспечивает превращение холестерина в прогестерон, способствуя синтезу P4. Эти данные свидетельствуют о том, что витамин D способен стимулировать развитие фолликулов за счёт повышения экспрессии CYP11A1 и усиления использования холестерина для синтеза прогестерона.
Витамин D3 способствует возобновлению мейоза ооцитов за счёт ингибирования сигнального пути TGF-β1. Кроме того, витамин D3 способен ослаблять ингибирующее влияние избытка тестостерона на CX43. LH подавляет сигнальный путь TGF-β1, тогда как FSH, напротив, активирует его.
Витамин D3 стимулирует пролиферацию гранулёзных клеток посредством повышения экспрессии мРНК CDK4 и CyclinD1 и подавления экспрессии мРНК P21. Он также усиливает секрецию E2 и P4 гранулёзными клетками за счёт стимуляции экспрессии ферментов стероидогенеза, тем самым способствуя развитию фолликулов.
Кроме того, витамин D3 снижает синтез мРНК AMHR-II посредством ингибирования фосфорилирования SMAD 1/5/8. За счёт повышения уровней SOD и CAT витамин D3 уменьшает образование ROS, оказывая противовоспалительное действие и снижая негативное влияние оксидативного стресса на развитие фолликулов.
Недавно было показано, что добавление витамина D3 в рацион кур-несушек приводило к значительному повышению уровня P4 в сыворотке крови при одновременном снижении уровня общего холестерина.
В дальнейшем установлено, что после 24 часов культивирования фолликулов кур in vitro с витамином D3 (10 нМ и 100 нМ) уровни P4 в гранулёзных и тека-клетках значительно повышались. Дополнительный ПЦР-анализ показал, что витамин D3 в концентрации 10 нМ существенно повышал уровень мРНК CYP11A1.
Фермент, кодируемый CYP11A1, обеспечивает превращение холестерина в прогестерон, способствуя синтезу P4. Эти данные свидетельствуют о том, что витамин D способен стимулировать развитие фолликулов за счёт повышения экспрессии CYP11A1 и усиления использования холестерина для синтеза прогестерона.
Рис.3
(TGF-β1 — трансформирующий фактор роста β; NPPC — натрийуретический пептид типа C; Cx43 — коннексин 43; CDK4 — циклин-зависимая киназа 4; E2 — эстрадиол; P4 — прогестерон; SOD — супероксиддисмутаза; CAT — каталаза; ROS — активные формы кислорода. Красные стрелки обозначают стимуляцию, синие — ингибирование.)
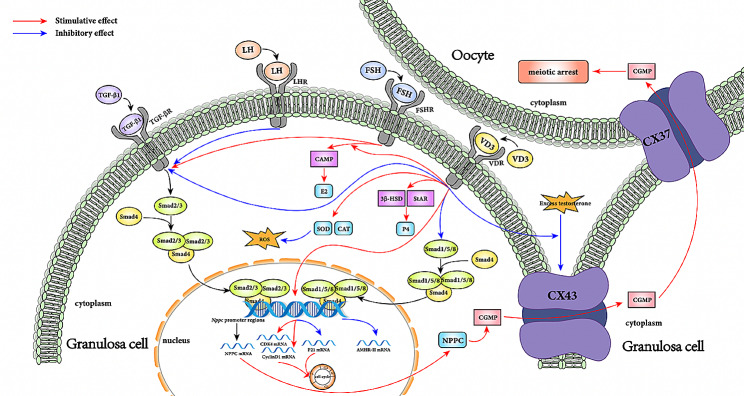
Противовоспалительные эффекты
Регуляция фолликулогенеза витамином D3 связана не только с усилением поддержки со стороны различных молекул и гормонов, но и со снижением воздействия неблагоприятных факторов, влияющих на развитие фолликулов, включая активные формы кислорода (ROS) и конечные продукты гликирования (AGEs).
Оксидативный стресс является одним из факторов, запускающих старение ооцитов. Он может приводить к нарушению формирования антральных фолликулов и аномалиям мейоза ооцитов, тем самым негативно влияя на развитие фолликулов.
В рандомизированном контролируемом исследовании с участием 60 пациенток с СПКЯ показано, что добавление витамина D-K-кальция значительно повышало общую антиоксидантную способность плазмы (TAC) и снижало концентрацию малонового диальдегида (MDA). Однако в данной работе отдельно не анализировались эффекты витамина D3 и его концентрации у пациенток с СПКЯ.
Оксидативный стресс является одним из факторов, запускающих старение ооцитов. Он может приводить к нарушению формирования антральных фолликулов и аномалиям мейоза ооцитов, тем самым негативно влияя на развитие фолликулов.
В рандомизированном контролируемом исследовании с участием 60 пациенток с СПКЯ показано, что добавление витамина D-K-кальция значительно повышало общую антиоксидантную способность плазмы (TAC) и снижало концентрацию малонового диальдегида (MDA). Однако в данной работе отдельно не анализировались эффекты витамина D3 и его концентрации у пациенток с СПКЯ.
Позднее было показано, что применение только витамина D3 (10 нМ) значительно снижало уровень ROS в гранулёзных клетках коз и повышало уровни мРНК и белков антиоксидантных ферментов — супероксиддисмутазы 2 (SOD2) и каталазы (CAT).
Это указывает на то, что витамин D3 снижает уровень ROS и способствует пролиферации гранулёзных клеток через усиление экспрессии SOD и CAT.Недавно в модели гранулёзоподобных опухолевых клеток, индуцированных высоким уровнем андрогенов для имитации изменений гранулёзных клеток при СПКЯ, показано, что витамин D3 (100 нМ) эффективно подавлял повышение уровней MDA, ROS и перекисного окисления липидов, вызванное гиперандрогенией. Это сопровождалось снижением оксидативного стресса и повышением жизнеспособности гранулёзных клеток, что открывает новые перспективы применения витамина D3 в терапии СПКЯ.
Конечные продукты гликирования (AGEs) представляют собой цитотоксические метаболические продукты, которые связываются с рецептором RAGE на гранулёзных и тека-клетках, вызывая клеточную дисфункцию и нарушения роста фолликулов.
В исследованиях на крысах, получавших рацион с высоким содержанием AGEs, наблюдалось снижение уровней E2 и P4 и повышение уровня тестостерона, тогда как экспрессия RAGE снижалась примерно на 30%, что свидетельствует о негативном влиянии AGEs на развитие фолликулов через нарушение синтеза стероидных гормонов.
Кроме того, показано, что AGEs способны нарушать внутриклеточную передачу сигналов инсулина и транспорт глюкозы в гранулёзных клетках, приводя к нарушениям фолликулогенеза.
Растворимый рецептор sRAGE конкурирует со свободными AGEs за связывание и тем самым оказывает ингибирующее действие [65]. Витамин D3 значительно повышает уровень sRAGE в яичниках, снижая негативное влияние накопления AGEs в гранулёзных и тека-клетках на развитие фолликулов.
Также установлена тесная связь витамина D3 с осью AGE-RAGE. В модели гематоэнцефалического барьера in vitro витамин D3 подавлял воспалительные реакции, индуцированные AGEs.
Исследования на человеческих гранулёзных клетках in vitro показали, что витамин D3 ослабляет влияние AGEs на экспрессию генов, связанных со стероидогенезом в лютеинизированных гранулёзных клетках, в частности подавляет индуцированное AGEs повышение уровней мРНК CYP11A1, StAR и CYP17A1.
Кроме того, показано, что AGEs усиливают фосфорилирование SMAD 1/5/8, индуцированное рекомбинантным AMH, тогда как добавление витамина D3 нивелирует этот эффект и подавляет вызванное AGEs повышение уровня мРНК AMHR-II.
Эти данные свидетельствуют о том, что витамин D3 способен поддерживать нормальное развитие фолликулов за счёт снижения активности AGEs. Однако исследования проводились преимущественно на лютеинизированных гранулёзных клетках после стимуляции овуляции у пациенток ЭКО, без оценки влияния витамина D3 на нелютеинизированные гранулёзные клетки, что требует дальнейшего изучения.
Это указывает на то, что витамин D3 снижает уровень ROS и способствует пролиферации гранулёзных клеток через усиление экспрессии SOD и CAT.Недавно в модели гранулёзоподобных опухолевых клеток, индуцированных высоким уровнем андрогенов для имитации изменений гранулёзных клеток при СПКЯ, показано, что витамин D3 (100 нМ) эффективно подавлял повышение уровней MDA, ROS и перекисного окисления липидов, вызванное гиперандрогенией. Это сопровождалось снижением оксидативного стресса и повышением жизнеспособности гранулёзных клеток, что открывает новые перспективы применения витамина D3 в терапии СПКЯ.
Конечные продукты гликирования (AGEs) представляют собой цитотоксические метаболические продукты, которые связываются с рецептором RAGE на гранулёзных и тека-клетках, вызывая клеточную дисфункцию и нарушения роста фолликулов.
В исследованиях на крысах, получавших рацион с высоким содержанием AGEs, наблюдалось снижение уровней E2 и P4 и повышение уровня тестостерона, тогда как экспрессия RAGE снижалась примерно на 30%, что свидетельствует о негативном влиянии AGEs на развитие фолликулов через нарушение синтеза стероидных гормонов.
Кроме того, показано, что AGEs способны нарушать внутриклеточную передачу сигналов инсулина и транспорт глюкозы в гранулёзных клетках, приводя к нарушениям фолликулогенеза.
Растворимый рецептор sRAGE конкурирует со свободными AGEs за связывание и тем самым оказывает ингибирующее действие [65]. Витамин D3 значительно повышает уровень sRAGE в яичниках, снижая негативное влияние накопления AGEs в гранулёзных и тека-клетках на развитие фолликулов.
Также установлена тесная связь витамина D3 с осью AGE-RAGE. В модели гематоэнцефалического барьера in vitro витамин D3 подавлял воспалительные реакции, индуцированные AGEs.
Исследования на человеческих гранулёзных клетках in vitro показали, что витамин D3 ослабляет влияние AGEs на экспрессию генов, связанных со стероидогенезом в лютеинизированных гранулёзных клетках, в частности подавляет индуцированное AGEs повышение уровней мРНК CYP11A1, StAR и CYP17A1.
Кроме того, показано, что AGEs усиливают фосфорилирование SMAD 1/5/8, индуцированное рекомбинантным AMH, тогда как добавление витамина D3 нивелирует этот эффект и подавляет вызванное AGEs повышение уровня мРНК AMHR-II.
Эти данные свидетельствуют о том, что витамин D3 способен поддерживать нормальное развитие фолликулов за счёт снижения активности AGEs. Однако исследования проводились преимущественно на лютеинизированных гранулёзных клетках после стимуляции овуляции у пациенток ЭКО, без оценки влияния витамина D3 на нелютеинизированные гранулёзные клетки, что требует дальнейшего изучения.

Клиническое применение
Витамин D3 играет важную роль в развитии фолликулов, что тесно связано с заболеваниями женской репродуктивной системы и фертильностью.
В двойном слепом многоцентровом исследовании с участием 750 женщин с СПКЯ показано, что у пациенток с дефицитом витамина D3 (<20 нг/мл) овуляция происходила реже, а частота живорождения была ниже по сравнению с женщинами с нормальным уровнем витамина D3.
Метаанализ девяти рандомизированных контролируемых исследований показал, что добавление витамина D3 по сравнению с плацебо или метформином значительно стимулировало развитие фолликулов и увеличивало число доминантных фолликулов (OR = 2,34; 95% ДИ: 1,39–3,92), что в итоге улучшало показатели наступления беременности.
Однако в другом двойном слепом плацебо-контролируемом исследовании с участием 123 пациенток с СПКЯ добавление витамина D3 не оказало значимого влияния на метаболические и эндокринные показатели.
Вероятно, такие различия связаны с дозировками витамина D3 и особенностями исследуемых групп. Необходимы крупные долгосрочные рандомизированные исследования высокого качества для определения пороговых эффектов витамина D в отношении гормональных, метаболических и репродуктивных показателей у пациенток с СПКЯ, а также для оценки влияния дозировки, способа введения и времени назначения витамина D3 на эффективность терапии.
Ранее показано, что у мышей с дефицитом витамина D3 фертильность снижалась на 75%, а число живорождений — на 30% по сравнению с контрольной группой. Кроме того, дефицит витамина D3 у матерей отрицательно влиял на репродуктивную функцию потомства, что проявлялось снижением овуляции и удлинением и нерегулярностью эстрального цикла во взрослом возрасте.Также в ряде исследований выявлена обратная связь между уровнем витамина D3 и АМГ — маркером овариального резерва.Ранее было показано, что витамин D3 способен напрямую усиливать секрецию прогестерона гранулёзными клетками яичников in vitro. Это позволяет предположить, что витамин D3 может поддерживать имплантацию эмбриона и снижать риск выкидыша за счёт стимуляции синтеза прогестерона в ранние сроки беременности, тем самым способствуя повышению фертильности.
Уровень витамина D3 также влияет на результаты программ экстракорпорального оплодотворения (ЭКО). В проспективном исследовании с участием 80 женщин с бесплодием, проходивших IVF/ICSI, показано, что витамин D3 независимо повышал частоту имплантации и эффективность ЭКО, не влияя при этом на количество и качество ооцитов. В другом проспективном когортном исследовании с участием 84 женщин, проходивших ЭКО, у пациенток с высоким исходным уровнем витамина D вероятность успешного исхода ЭКО была в четыре раза выше по сравнению с женщинами с низким уровнем витамина D (p < 0,01). Многофакторный логистический анализ подтвердил, что уровень 25(OH)D в фолликулярной жидкости является независимым предиктором успешного цикла ЭКО.
Предполагается, что витамин D3 влияет не только на развитие фолликулов, но и на процессы оплодотворения и имплантации эмбриона, тем самым определяя исходы ЭКО. Однако для точного понимания роли и механизмов действия витамина D3 в программах ЭКО необходимы дополнительные исследования.
В двойном слепом многоцентровом исследовании с участием 750 женщин с СПКЯ показано, что у пациенток с дефицитом витамина D3 (<20 нг/мл) овуляция происходила реже, а частота живорождения была ниже по сравнению с женщинами с нормальным уровнем витамина D3.
Метаанализ девяти рандомизированных контролируемых исследований показал, что добавление витамина D3 по сравнению с плацебо или метформином значительно стимулировало развитие фолликулов и увеличивало число доминантных фолликулов (OR = 2,34; 95% ДИ: 1,39–3,92), что в итоге улучшало показатели наступления беременности.
Однако в другом двойном слепом плацебо-контролируемом исследовании с участием 123 пациенток с СПКЯ добавление витамина D3 не оказало значимого влияния на метаболические и эндокринные показатели.
Вероятно, такие различия связаны с дозировками витамина D3 и особенностями исследуемых групп. Необходимы крупные долгосрочные рандомизированные исследования высокого качества для определения пороговых эффектов витамина D в отношении гормональных, метаболических и репродуктивных показателей у пациенток с СПКЯ, а также для оценки влияния дозировки, способа введения и времени назначения витамина D3 на эффективность терапии.
Ранее показано, что у мышей с дефицитом витамина D3 фертильность снижалась на 75%, а число живорождений — на 30% по сравнению с контрольной группой. Кроме того, дефицит витамина D3 у матерей отрицательно влиял на репродуктивную функцию потомства, что проявлялось снижением овуляции и удлинением и нерегулярностью эстрального цикла во взрослом возрасте.Также в ряде исследований выявлена обратная связь между уровнем витамина D3 и АМГ — маркером овариального резерва.Ранее было показано, что витамин D3 способен напрямую усиливать секрецию прогестерона гранулёзными клетками яичников in vitro. Это позволяет предположить, что витамин D3 может поддерживать имплантацию эмбриона и снижать риск выкидыша за счёт стимуляции синтеза прогестерона в ранние сроки беременности, тем самым способствуя повышению фертильности.
Уровень витамина D3 также влияет на результаты программ экстракорпорального оплодотворения (ЭКО). В проспективном исследовании с участием 80 женщин с бесплодием, проходивших IVF/ICSI, показано, что витамин D3 независимо повышал частоту имплантации и эффективность ЭКО, не влияя при этом на количество и качество ооцитов. В другом проспективном когортном исследовании с участием 84 женщин, проходивших ЭКО, у пациенток с высоким исходным уровнем витамина D вероятность успешного исхода ЭКО была в четыре раза выше по сравнению с женщинами с низким уровнем витамина D (p < 0,01). Многофакторный логистический анализ подтвердил, что уровень 25(OH)D в фолликулярной жидкости является независимым предиктором успешного цикла ЭКО.
Предполагается, что витамин D3 влияет не только на развитие фолликулов, но и на процессы оплодотворения и имплантации эмбриона, тем самым определяя исходы ЭКО. Однако для точного понимания роли и механизмов действия витамина D3 в программах ЭКО необходимы дополнительные исследования.
Заключение
Сообщается, что дефицит витамина D3 среди женщин встречается всё чаще. При этом недостаточность витамина D3 оказывает выраженное неблагоприятное влияние на женскую репродуктивную систему, включая развитие СПКЯ, снижение фертильности и ухудшение результатов вспомогательных репродуктивных технологий. В связи с этим добавление витамина D3 рассматривается как простой, доступный и экономически целесообразный способ коррекции этих нарушений.
Однако для рационального клинического применения витамина D3 необходимо более глубокое понимание механизмов его действия в процессе фолликулогенеза.
Витамин D3 локально синтезируется в фолликулах, а рецепторы VDR широко представлены в их структуре, что указывает на тесную связь витамина D3 с процессами развития фолликулов. Совокупность имеющихся данных свидетельствует о потенциальной роли витамина D3 на всех этапах фолликулогенеза — от активации примордиальных фолликулов до формирования доминантного фолликула, его дальнейшего роста и созревания. Кроме того, витамин D3 стимулирует пролиферацию гранулёзных клеток и рост фолликулов на поздних стадиях развития.
В данном обзоре обобщены данные о влиянии витамина D3 на развитие фолликулов и возможных механизмах его действия. Витамин D3 способствует фолликулогенезу через регуляцию молекул, участвующих в мейозе ооцитов и секреции стероидных гормонов гранулёзными клетками.
С одной стороны, витамин D3 способен ослаблять негативное влияние избытка тестостерона на межклеточные контакты между гранулёзными клетками, поддерживать транспорт циклического гуанозинмонофосфата (cGMP) и способствовать выходу ооцитов из состояния мейотического ареста.
С другой стороны, витамин D3 снижает экспрессию TGF-β1 в гранулёзных клетках, тем самым подавляя TGF-β1-опосредованный мейотический арест и стимулируя развитие ооцитов.
Кроме того, витамин D3 усиливает пролиферацию гранулёзных клеток за счёт регуляции экспрессии генов клеточного цикла. Также показано, что витамин D3 обладает антиоксидантными и антиапоптотическими свойствами, обеспечивая защиту фолликулов.
Это имеет значение не только для обоснованного применения витамина D3 при заболеваниях женской репродуктивной системы, например для улучшения овуляции у пациенток с СПКЯ, но и для повышения эффективности вспомогательных репродуктивных технологий.
Использование витамина D3 в средах культивирования ооцитов до и после криоконсервации может повышать степень созревания ооцитов in vitro, что представляет интерес для дальнейшего развития вспомогательных репродуктивных технологий.
Однако из-за сложностей сохранения и культивирования ранних фолликулов in vitro механизмы действия витамина D3 на ранние стадии фолликулогенеза остаются недостаточно изученными. В связи с этим необходимы дополнительные исследования, направленные на изучение детальных сигнальных путей витамина D3 в развитии ооцитов ранних фолликулов и созревании фолликулов.
Кроме того, общий эффект добавления витамина D3 на функцию яичников in vivo зависит от исходного уровня витамина D у пациенток, а также от формы, дозировки и времени назначения витамина D. Поэтому для дальнейшего изучения этих вопросов всё ещё необходимы дополнительные рандомизированные контролируемые исследования.
Однако для рационального клинического применения витамина D3 необходимо более глубокое понимание механизмов его действия в процессе фолликулогенеза.
Витамин D3 локально синтезируется в фолликулах, а рецепторы VDR широко представлены в их структуре, что указывает на тесную связь витамина D3 с процессами развития фолликулов. Совокупность имеющихся данных свидетельствует о потенциальной роли витамина D3 на всех этапах фолликулогенеза — от активации примордиальных фолликулов до формирования доминантного фолликула, его дальнейшего роста и созревания. Кроме того, витамин D3 стимулирует пролиферацию гранулёзных клеток и рост фолликулов на поздних стадиях развития.
В данном обзоре обобщены данные о влиянии витамина D3 на развитие фолликулов и возможных механизмах его действия. Витамин D3 способствует фолликулогенезу через регуляцию молекул, участвующих в мейозе ооцитов и секреции стероидных гормонов гранулёзными клетками.
С одной стороны, витамин D3 способен ослаблять негативное влияние избытка тестостерона на межклеточные контакты между гранулёзными клетками, поддерживать транспорт циклического гуанозинмонофосфата (cGMP) и способствовать выходу ооцитов из состояния мейотического ареста.
С другой стороны, витамин D3 снижает экспрессию TGF-β1 в гранулёзных клетках, тем самым подавляя TGF-β1-опосредованный мейотический арест и стимулируя развитие ооцитов.
Кроме того, витамин D3 усиливает пролиферацию гранулёзных клеток за счёт регуляции экспрессии генов клеточного цикла. Также показано, что витамин D3 обладает антиоксидантными и антиапоптотическими свойствами, обеспечивая защиту фолликулов.
Это имеет значение не только для обоснованного применения витамина D3 при заболеваниях женской репродуктивной системы, например для улучшения овуляции у пациенток с СПКЯ, но и для повышения эффективности вспомогательных репродуктивных технологий.
Использование витамина D3 в средах культивирования ооцитов до и после криоконсервации может повышать степень созревания ооцитов in vitro, что представляет интерес для дальнейшего развития вспомогательных репродуктивных технологий.
Однако из-за сложностей сохранения и культивирования ранних фолликулов in vitro механизмы действия витамина D3 на ранние стадии фолликулогенеза остаются недостаточно изученными. В связи с этим необходимы дополнительные исследования, направленные на изучение детальных сигнальных путей витамина D3 в развитии ооцитов ранних фолликулов и созревании фолликулов.
Кроме того, общий эффект добавления витамина D3 на функцию яичников in vivo зависит от исходного уровня витамина D у пациенток, а также от формы, дозировки и времени назначения витамина D. Поэтому для дальнейшего изучения этих вопросов всё ещё необходимы дополнительные рандомизированные контролируемые исследования.




ООО «Мидика Рус» Россия, 143 090, Московская область,
г. Краснознаменск, ул. Строителей, дом 17, офис 14
СГР № АМ.01.06.01.003.R.87.09.20 от 02.09.2020 г. ТУ 10.89.19−117−71 892 692−2020
ИНН: 5032375192 ОГРН: 503201001
БАД. Не является лекарственным средством
















